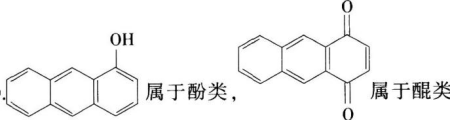
下列每组物质中含有的化学键类型相同的是( )。
下列实验现象描述的不合理的是( )。
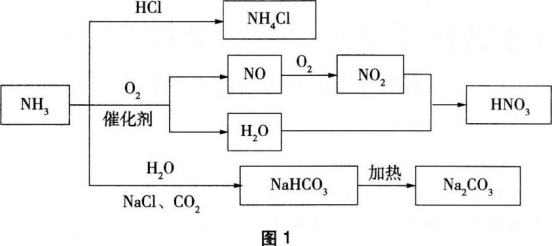
NH3是一种重要的化学原料,可以制备一系列物质(如图1)。下列有关表述正确的是( )。
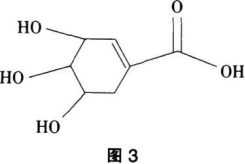
莽草酸结构简式如图3。下列说法错误的是( )。
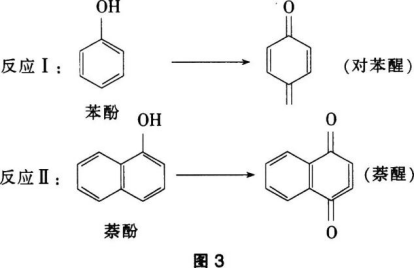
醌类化合物广泛存在于植物中,有抑菌、杀菌作用,可由酚类物质制备。 下列说法不正确的是( )。
下列关于常见有机化合物的说法正确的是( )。
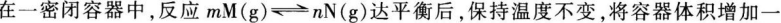
倍,当达到新的平衡时,N的浓度是原平衡的70%,则( )。
某化学老师在一次化学测验中设计了下列试题.并对部分学生的解题结果进行了统计和分析。 【试题】X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为Z2-和Z-,Y+和Z-离子具有相同的电子层结构。下列说法正确的是( )。 A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z C.离子半径:X2->Y+>Z- D.原子序数:X>Y>Z 【考试结果】对参加考试的全体考生的答案情况统计如下:

试根据上述信息,回答下列问题:
本题正确的选项是什么?
请分析和诊断各个选项解答的错误原因。
如果你要讲评本题,你教给学生的正确解题思路是什么?
某化学教师在一次化学测验中设计了下列试题,并对部分学生的考试结果进行了统计和分析。 【试题】下列叙述中,正确的是( )。

本题的正确答案是____________。
如果你要讲解本题,请写出你的正确解题思路。
请对学生答题错误的原因进行分析和诊断。
某化学教师在一次化学测验中设计了下面试题,并对学生的解题结果进行了统计和分析。【试题】用酸性氢氧燃料电池为电源进行电解的实验装置如图5所示,下列说法正确的是( )。
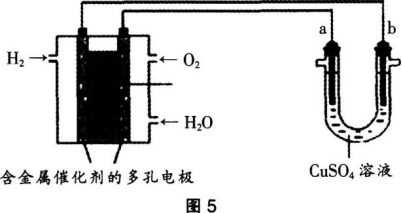
A.燃料电池工作时,正极反应为O2+2H2O+4e-=4OH-
B.电解精炼铜时,若转移1mol电子,a极质量减少32g
C.铁表面镀铜时,a为铁,b为铜
D.若a,b两极为石墨,相同条件下,a极产生气体与电池中消耗的氧气体积相同【考试结果】对参加考试的全体学生的答题情况统计如表1所示:
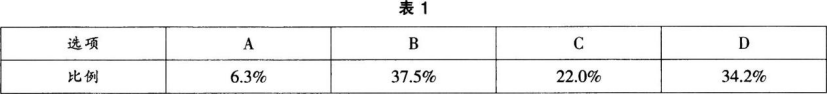
试根据上述信息,回答下列问题:
本题的正确选项是什么?
请分析其余三个选项,并诊断学生解答错误的原因。
如果要你讲评本题,你教给学生的正确解题方法是什么?
根据下列材料,按要求完成任务。
材料一《普通高中课程标准(实验)》的内容标准:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要应用。
材料二“铁的重要化合物”内容属于高中化学必修阶段的无机元素化合物教学内容,必修化学课程中的无机元素化合物知识安排在《化学1》的“主题3常见无机物及其应用”中。普通高中课程标准使用教科书《化学1》的目录:
第一章从实验学化学
第二章化学物质及其变化
第三章金属及其化合物
第一节金属的化学性质
第二节几种重要的金属化合物
第三节用途广泛的金属材料
第四章非金属及其化合物
材料三以下是某教师设计的教学活动:
【学生活动】阅读教材关于铁的氧化物的介绍,利用分类法归纳FeO、Fe2O3、Fe3O4的性质,并填写表格。
【学生实验1】氢氧化铁、氢氧化亚铁的制备与Fe3+离子检验(整合实验)。
【问题情景1】阅读课文,结合实验现象,思考与讨论:
1.利用KSCN溶液,可以根据什么现象检验溶液中Fe3+的存在?Fe2+离子遇到KSCN会产生相同的现象吗?
2.FeSO4溶液滴加KSCN溶液一段时间后,再次观察溶液的颜色,出现了什么变化?该变化说明了什么?由此你可以得出什么结论?
3.Fe(OH)2沉淀是什么颜色?为什么往FeSO。溶液中滴加NaOH溶液后生成的沉淀会出现
颜色变化?
【师生小结】
【问题情景2】
1.从Fe2+被O2氧化为Fe3+,体现了Fe2+的什么性质?除了O2,还有哪些物质可以氧化Fe2+?
2.若要实现从Fe3+转为Fe2+的变化,需要加入什么物质?
【学生实验2】Fe2+与Fe3+的转化,按照教材P61科学探究进行实验,观察与记录实验现象。
【问题情景3】结合实验探究的现象,思考与讨论:
1.Fe3+与铁粉充分反应后的产物是什么?如何证明?
2.回忆前面有关Fe2+的实验,为什么用Fe与稀硫酸制备FeSO4溶液,并保持铁过量?
3.实验中如何判断Fe3+已充分反应?反应不充分对实验结果有何影响?
【师生小结】
【问题情景3】学生课后思考与讨论
通过学习我们知道,Fe2+离子和Fe(OH)2中+2价的铁均易被氧化。根据所学的知识,思考:
利用FeSO4溶液和NaOH溶液时,如何通过实验条件的控制,制备较纯净的Fe(OH)2白色沉淀?
请根据上述材料,完成“铁的化合物”这一教学片段的有关任务:
试确定本课的三维教学目标。
说明本节课的教学策略。
请对本课内容进行板书设计。
请对本课内容设计导入。
请写出氢氧化铁、氢氧化亚铁的制备与检验Fe3+离子的实验步骤。
案例:
下面是两位中学教师关于“酯化反应”的教学过程实录。李老师的教学实录
【播放漫画】看漫画,喝醋能解酒。
【讲述】台州人以豪爽著称,经常以酒会友,为什么喝醋能够解酒?
【回答】酸跟醇作用生成酯。
【讲述】同学们回答的很对,大家经过预习已经知道酸跟醇作用生成酯。下面让我们用实验来解释一下这个原理吧。
【活动与探究的讲述】实验的第一步是什么?反应所需的药品是什么?各起什么作用?药品的添加顺序如何?浓硫酸的作用是什么?得到的反应产物是否纯净?主要杂质有哪些?如何除去?用什么来吸收乙酸乙酯?
【实验探究】学生分组讨论,制定实验方案,老师巡回检查,以保证实验安全。
【讲述】像这种酸和醇作用,生成酯和水的反应叫作酯化反应。该反应是可逆反应。
【投影】【思考探究】反应中是乙醇中的C2H5O-取代了乙酸中-OH的位置,还是乙醇中的C2H5-取代了乙酸中H-的位置?
【讲述】生物学家们为了研究海豚或某类鱼的活动情况,常采用的方法是将一个跟踪器安装在其身体某部位。同样在化学上我们也可以用一个跟踪器安装在分子里,这种方法称为同位素示踪法。例如将含18O醇与乙酸反应。反应后,18O在乙酸乙酯的位置。证明,乙酸乙酯是乙醇分子中的乙氧基(C2H5O-)取代了乙酸分子中羧基上的羟基(-OH)的生成物。
【课后作业布置】绍兴女儿红非常有名,为什么酒越陈越香,同学们课后想一想?
王老师的教学实录
【投影】
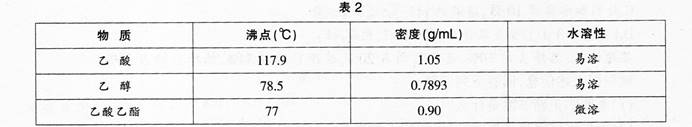
【演示实验】乙酸与乙醇的反应
【讲解】通过实验得出:乙酸与乙醇在有浓硫酸存在并加热的条件可以发生反应,实验中生成的有果香味的无色透明油状液体叫乙酸乙酯。像这种酸跟醇作用生成酯和水的反应叫酯化反应。乙酸与乙醇的酯化反应是可逆的。
【投影思考】
1.为什么导管不插入饱和Na2CO3溶液中?
2.反应原理是什么?
3.浓硫酸的作用是什么?
4.盛饱和Na2CO3溶液的试管中的现象是什么?
5.饱和Na2CO3溶液有什么作用?
【过渡】在上述这个酯化反应中,生成物水中的氧原子是由乙酸分子中的羧基上的羟基提供?还是由乙醇分子的羟基提供?如何能证明你的判断是正确的?能否提供理论或实验依据?
【提问】在酯化反应中乙酸和乙醇有几种可能的断键方式?如何确定实际发生的是哪种断键方式?
【回答】两种可能的断键情况
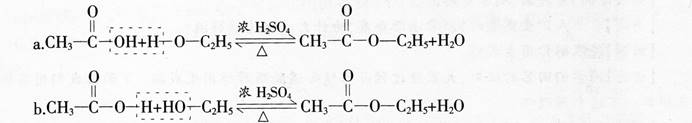
【讲述】用含18O的醇跟羧酸起酯化反应,形成含有18O的酯,证明这种酯化反应的实质是:羧酸脱去羧基上的羟基,醇脱去羟基上的氢原子。
【动画演示】利用同位素原子示踪法验证酯化反应的实质。
【板书】略。
根据两位老师的教学过程,说明各自所用教学方法的优点。
以李老师的教学为例,说明化学实验对发展学生科学素养具有哪些作用。
根据上述教学实例,归纳总结出化学反应原理这一类知识的基本教学思路。