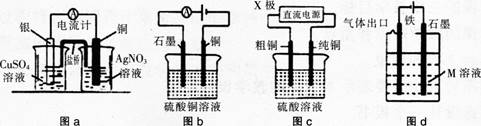
有关下列电化学装置的说法中正确的是( )。
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )。
某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定
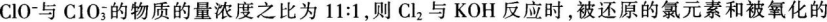
氯元素的物质的量之比为( )。
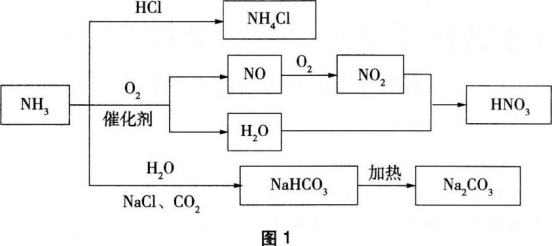
NH3是一种重要的化学原料,可以制备一系列物质(如图1)。下列有关表述正确的是( )。
盐酸乙哌立松片(Eperisone Hydrochloride Tablets)是种骨骼肌松弛剂,能改善由肩周
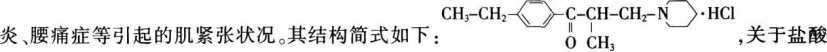
乙哌立松片有下列说法: ①是芳香族化合物 ②含有N原子的六元环上所有原子均处于同一平面 ③是一种有机盐 ④能发生还原反应的官能团或原子团有两种 其中正确的是( )。
①文献法②观察法③调查法④实验法
阅读下列材料,回答相关问题。
《普通高中化学课程标准(实验)》中指出,“实验化学”是普通高中化学课程的重要组成部分。设置该课程模块有助于学生更深刻地认识实验在化学中的地位,掌握基本的化学实验方法和技能,培养学生的创新精神和实践能力。
根据材料,请回答以下问题:
化学实验方案设计的基本要求是什么?
化学实验方案设计的一般思路是什么?
通过该模块的学习,学生可以得到哪些发展?
阅读下面材料,回答相关问题。 1.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。 Ⅱ.某课外活动小组利用图5装置进行乙醇的催化氧化实验并制取乙醛。图4中铁架台等装置已略去。粗黑线表示乳胶管。
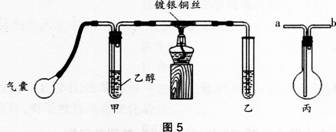
根据上述材料回答问题:
课本中实验制取乙醛存在哪些不足?
Ⅱ实验中,为了使反应进行的速率加快,需增加什么装置?
教师在设计实验教学活动时,应如何培养学生的创新能力?
根据下列材料.按要求完成任务。
材料一《普通高化学课程标准(实验)》内容标准:以酸雨的防治和无磷洗涤剂的使用为例,体会化学对环境保护的意义:能说明合成新物质对人类生活的影响,讨论在化工生产中遵循“绿色化学”思想的重要性。
材料二某版本教科书《化学2》(必修)的知识结构体系
第一章物质结构元素周期律
第二章化学反应与能量
第三章有机化合物
第四章化学与自然资源的开发利用
第一节开发利用金属矿物和海水资源
第二节资源综合利用环境保护
材料三某版本教科书《化学2》“环境保护与绿色化学”的片段:

通常所说的环境问题,主要是指由于人类不合理地开发和和用自然资源而造成的生态环境破坏.以及工农业生产和人类生活所造成的环境污染。对环境情况的监测、兰废的治理、寻找源头治理环境污染的生产工艺等.都是当今化学工 作者面临的重要任务。
要了解环境的污染情况,消除和控制污染以及研究污染物的存在、分布和转化规律.就需要对污染物的存在形态、含量等进行分析和鉴定.提供可靠的分析数据。化学工作者芷承担着繁重的环境监测工作。

除了自然因素外.大气污染物主要来自化石燃料燃烧和工业生产过程产生的废气及其携带的颗粒物;工业生产中的废水(废液)往往含有复杂的成分.任意排放会导致土壤、水源的污染.需要经过多步处理才能达到排放标准;废渣等固体废弃物的处理兼有减少环境污染和资源回收利用两个霞要目的。化学在三废治理方面发挥着重要的作用。

1.硫氧化物和氮氧化物(NOx)是形成酸雨的主要物质。 工业上常利用它们与一些廉价易得的化学物质发生反应加以控制、消除或回收利用。请举例说明这些方法的化学反应原理和类型。
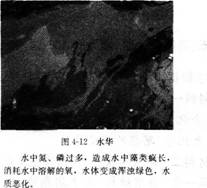
2.含氯、磷的大量污水任意排向湖泊、水库和近海海域.会出现水华、赤潮等水体污染问题。你认为在农村和城市造成的这种水体污染各有什么特点, 并请查阅资料了解有关的污染及治理情况
3.结合实例.分析和说明在化学实验中如何防止可能造成的室内和室外环境的污染。
我们可以设想。实施清洁生产既能满足人们的物质需求又可以合理使用翻然资源.同时可以保护环境。绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环罐的污染。

回答【思考与交流】中的问题1。
完成“环境保护与绿色化学’’的教学设计片段,内容包括教学目标、教学方法和教学过程。
阅读下列材料,按要求完成教学设计。 材料一《普通高中化学课程标准(2017年版)》关于“原子结构与元素周期律”的内容标准:体会元素周期律(表)在学习元素及其化合物知识及科学研究中的重要作用。 材料二某版本教材化学必修第一册第四章第二节“元素周期律”的部分内容: 二、元素周期表和元素周期律的应用 元素周期律的发现,对化学的发展有很大的影响。作为元素周期律表现形式的元素周期表,反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。 我们可以在周期表中给金属元素和非金属元素分区。如图4一13所示,虚线左下方是金属元素,虚线右上方是非金属元素,最右一个纵列是稀有气体元素。由于元素的金属性与非金属性之间并没有严格的界线,位于分界线附近的元素既能表现出一定的金属性,又能表现出一定的非金属性。在周期表中,主族元素从上到下、从左到右,元素的金属性和非金属性存在着一定的递变规律。
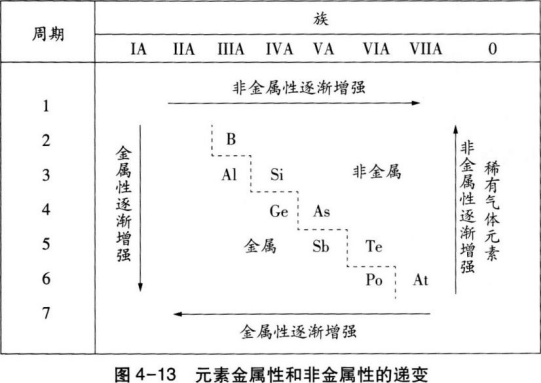
一般情况下,元素的化合价与元素在周期表中的位置有一定的关系。例如: 1.主族元素的最高正化合价等于它所处的族序数,因为族序数与最外层电子(价电子)数相同。 2.非金属元素的最高正化合价,等于原子所能失去或偏移的最外层电子数;而它的负化合价,则等于使原子达到8电子稳定结构所需得到的电子数。所以,非金属元素的最高正化合价和它的负化合价的绝对值之和等于8。 元素在周期表中的位置,反映了元素的原子结构和性质。在认识了元素周期律以后,可以根据元素在周期表中的位置推测其原子结构和性质,并研究元素性质的变化规律;也可以根据元素的原子结构推测其在周期表中的位置和性质。科学家依据元素周期律和周期表,对元素性质进行系统研究,可以为新元素的发现,以及预测它们的原子结构和性质提供线索。 由于周期表中位置靠近的元素性质相近,在一定区域内寻找元素、发现物质的新用途被视为一种相当有效的方法。例如,在周期表中金属与非金属的分界处可以找到半导体材料,如硅、锗、镓等。半导体器件的研制正是开始于锗,后来发展到研制与它同族的硅。又如,通常农药所含有的氟、氯、硫、磷、砷等元素在周期表中位置靠近,对这个区域内的元素进行研究,有助于制造出新品种的农药,如由含砷的有机物发展成对人畜毒性较低的含磷有机物等。人们还在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素?

材料三教学对象为高中一年级学生,学生已经学习了物质及其变化、海水中的重要元素——钠和氯、铁和金属材料、原子结构与元素周期表。 请完成材料二所示内容的教学设计(不少于300字)。
包含教学目标、教学重难点。
完成“元素周期表和元素周期律的应用”的教学设计过程。
阅读下列三段材料,根据要求完成任务。 材料一《普通高中化学课程标准(实验)》关于“离子反应”的内容标准:知道酸、碱、盐在溶液中能发生电离。 材料二某版高中必修教材《化学1》第二章第2节“离子反应”的部分内容:

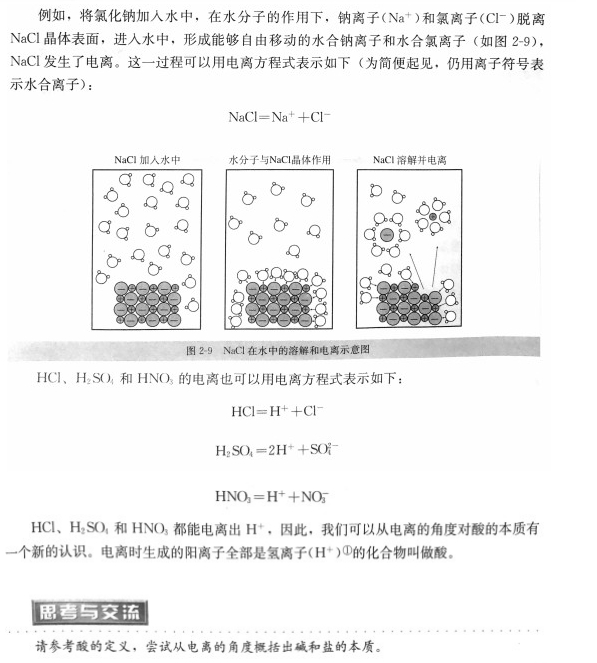
材料三教学对象为高一年级学生。学生在初三化学中已经学习了离子、盐酸、硫酸、氢氧化钠、氢氧化钙、氯化钠等知识。
关于电解质,学生易产生哪些错误认识?
根据以上材料完成“酸、碱、盐在水溶液中的电离”的教学设计,内容包括教学目标、教学重点、教学难点、教学方法、教学过程。(不少于300字)